Трэці закон тэрмадынамікі
| Законы тэрмадынамікі |
|---|

|
| Нулявы закон тэрмадынамікі |
| Першы закон тэрмадынамікі |
| Другі закон тэрмадынамікі |
| Трэці закон тэрмадынамікі |
Трэці пачатак тэрмадынамікі, трэці закон тэрмадынамікі, тэарэма Нэрнста — фізычны прынцып, які вызначае паводзіны энтрапіі сыстэмы пры набліжэньні тэмпэратуры да абсалютнага нуля. Зьяўляецца адным з пастулятаў тэрмадынамікі.
Фармулёўка: «прырашчэньне энтрапіі пры абсалютным нулі тэмпэратуры імкнецца да канцавога ліміту, які не залежыць ад таго, у якім раўнаважным стане знаходзіцца сыстэма».
або
дзе — любы тэрмадынамічны парамэтар.
Мінуўшчына[рэдагаваць | рэдагаваць крыніцу]
Першы і другі пачаткі тэрмадынамікі не дазваляюць вызначыць значэньне энтрапіі пры звышнізкіх значэньнях тэмпэратуры. На падставе абагульненьня экспэрымэнтальных дасьледваньняў уласьцівасьцяў розных рэчываў быў устаноўлены закон, які ліквідаваў гэты недахоп. Сфармуляваў яго ў 1906 року Вальтэр Нэрнст (1864—1941), гэты закон мае назву трэцяга пачатку тэрмадынамікі, ці тэарэмы Нэрнста. Тэарэму ў сучасны выгляд прывёў у 1911 Макс Плянк (1858—1947).
Прымяненьне[рэдагаваць | рэдагаваць крыніцу]
Тэарэма, базуючыся на квантамэханічных уяўленнях, можа быць выкарыстаная для вызначэньня дакладнай велічыні энтрапіі.
Дзе:
- — энтрапія сыстэмы [Дж/К],
- — колькасць мікрастанаў сыстэмы.
У клясычнай тэрмадынаміцы тэарэма Нэрнста мае абмежаваны ўжытак, бо, у асноўным, пры разьліках разглядаецца толькі адноснае зьмяненьне энтрапіі.
Высновы[рэдагаваць | рэдагаваць крыніцу]
Недасягальнасьць абсалютнага нуля тэмпэратуры[рэдагаваць | рэдагаваць крыніцу]
Недасягальнасьць абсалютнага нуля тэмпературы (-273,15 °C 0) можна растлумачыць:
1) У межах клясычнай тэрмадынамікі:
Пры абсалютным нулі тэмпэратуры энтрапія сыстэмы будзе роўная нулю:
Між іншым, гэта азначае магчымасьць стварэньня вечнага рухавіку другога роду з каэфіцыентам карыснага дзеяньня ў 100 адсоткаў:
што супярэчыць другому закону тэрмадынамікі.
2) Магчыма сфармуляваць прычыну недасягальнасьці абсалютнага нуля тэмпэратуры некалькі інакш:
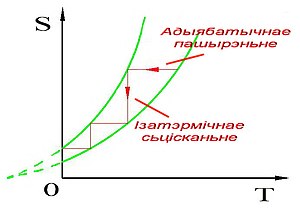
Калі сыстэма ахалоджваецца мэтадам паўтарэньня цыклю адыябатчнага пашырэньня (памяньшаецца тэмпэратура) і ізатэрмічнага сьцісканьня (памяньшаецца энтрапія), то пры набліжэньні значэньня да нуля энтрапія прымае значэньне нуля і больш ня зьмяняецца.
Гэта значыць, што пры канцавой колькасьці паўтарэньня цыкляў можна толькі асымптатычна (чым бліжэй да бясконцасьці, тым дакладней) набліжацца да стану з .
Часьцяком трэці пачатак тэрмадынамікі таксама мае фармулёўку, якая вынікае з гэтах двух пунктаў:
- «Абсалютны нуль тэмпэратуры недасягальны»
Паводзіны іншых фізычных велічыняў[рэдагаваць | рэдагаваць крыніцу]
Пры будуць таксама імкнуцца да нуля такія велічыні, як:
- — каэфіцыэнт цеплавога пашырэньня [K −1],
- — ізабарная цеплаёмістасьць [Дж/(кг·К)],
- — ізахорная цеплаёмістасьць [Дж/(кг·К)].
Глядзіце таксама[рэдагаваць | рэдагаваць крыніцу]
Літаратура[рэдагаваць | рэдагаваць крыніцу]
- Базаров И. П. Термодинамика — Москва: Высшая школа,1991, 376 с.
- Жилко В. В., Лавриненко А. В., Маркович Л. Г. Физика — Минск: Народная асвета, 2002, 382 с.

![{\displaystyle \lim \limits _{T\to \,0\,K}\left[S(T,x_{2})-S(T,x_{1})\right]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/70ddef8c496414b10d4ac0888d8758c4c79c42e5)













