Партал:Хімія/Абраная выява
Выкарыстаньне[рэдагаваць крыніцу]
Вывад гэтых падстаронак апрацоўваецца на старонцы Партал:Хімія/Абраная выява/Вывад.
- Дадаць новую выяву на падстаронку з наступным вольным нумарам.
- Абнавіць "max=" да новага значэньня шаблёну {{Выпадковы элемэнт парталу}} на асноўнай старонцы.
Сьпіс выбраных выяваў[рэдагаваць крыніцу]

Галь — хімічны элемэнт, які ў пэрыядычнай табліцы мае пазначэньне Ga і атамны лік 31. Рэдкі, мяккі серабрыста-мэталічны лёгкі мэтал, галь крохкі пры нізкіх тэмпэратурах, але пры тэмпэратурах вышэй за пакаёвую пачынае таяць нават у руках. Сустракаецца ў нязначнай колькасьці ў баксытах і цынкавых рудах. Выкарыстоўваецца для атрыманьня арсэніду галію, які прымяняецца як паўправаднік, асабліва ў сьвятлодыёдах.
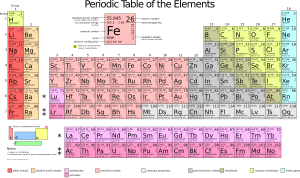
Пэрыядычная табліца хімічных элемэнтаў з назвамі, атамнымі масамі, электроннымі канфігурацыямі, першай энэргіяй іянізацыі і электраадмоўнасьцю.

Крышталі золата, сынтэзаваныя хімічным пераносам у хлёрнай атмасфэры. Чысьціня >99,99%

Ратавальнік авіяцыі Нацыянальнай гвардыі ЗША Тымаці Котэрал праходзіць дэзактывацыю пасьля спробы вызначыць некалькі біялягічных забруджвальнікаў у лябараторыі падчас вучэньняў „Глябальны цмок“-2015. Джорджыя, ЗША.

Выява паверхні нанакрысталічнага фасьфіду інду, атрыманага мэтадам электрахімічнага траўленьня. На паверхні сфармаваўся крысталічны аксыд індыю, які мае кветкападобную структуру. Фатаздымкі нанаструктураў атрымалі дасьледчыкі Бярдзянскага дзяржаўнага пэдагагічнага ўнівэрсытэту (Украіна) на растравым электронным мікраскопе JSM-6490 (павелічэньне ў 100 разоў). Нанаструктураваныя паўправаднікі выяўляюць шэраг незвычайных уласьцівасьцей, якімі не валодаў пачатковы паўправадніковы крыстал, таму іх часта называюць мэтаматэрыяламі або звышматэрыяламі.

Фрыдрых Вёлер (31 ліпеня 1800 — 23 верасьня 1882) — нямецкі хімік, вядомы сваім сынтэзам мачавіны, а таксама вылучэньнем некалькіх хімічны’ элемэнтаў. У 1828 року сваім здабыцьцём мачавіны зь неарганікі Вёлер давёў, што арганічныя рэчывы не абавязкова паходзяць зь біялягічных крыніцаў, абвергнуўшы дактрыну віталізму.

Трыёзафасфатмзамэраза — фэрмэнт, які каталізуе хуткую ізамэрызацыю гліцэральдэгід-3-фасфату ў дыгідрааксыацэтонфасфат.
Паклітаксэль — важны сродак пры лячэньні раку. Ягоная складаная будова стала складанай задачай пры спробе сынтэзу групай Кір’якаса Нікалаў. Колеры азначаюць спосабы, якія яны выпрабоўвалі.

Нафтаперапрацоўчая прамысловасьць — важная крыніца папаўненьня хімічнай сыравіны. На выяве паказаныя цыстэрны для захоўваньня нафты перапрацоўчага заводу MiRO ў Карльсруэ (Нямеччына).

Сульфат медзі — адно з самых вядомых злучэньняў медзі. У прыродзе яно сустракаецца ў выглядзе мінэралу халькантыту. На выяве рэчыва ў пэнтагідратнай форме.

Род — рэдказямельны серабрысты бліскучы мэтал. У парашкаватым выглядзе мае цёмны колер. Назва паходзіць ад грэцкага ῥόδον (ружа) — некаторыя злучэньні роду маюць чырвоны колер. На выяве прадстаўлены 1 г роду ў парашку, у спрэсаваным выглядзе і пасьля пераплаўкі газа-вальфрамавай дугой.

Перамяненьне вапняку ў нягашаную вапну (аксыд кальцу) рабілі яшчэ ў Старажытным Эгіпце, але і дагэтуль гэты працэс застаецца патрэбным. На выяве паказаная традыцыйна вапнапальная печ пад Антуанам (Бэльгія).

Газавая храматаграфія — важны від храматаграфіі, які прымяняецца ў хімічным аналізе. На выяве печ (з адкрытымі дзьвярыма), якая трымае патрэбную тэмпэратуру лятучага рэчыва.

Фэрамагнітная вадкасьць (у аліве) зьбіраецца да палюсоў магутнага магніту.
Флюарэсцэнцыя і падвойнае праменяпераламленьне сіняга лазэру з даўжынёю хвалі 445 нм у крышталі кальцыту.

Хімічныя танкеры займаюцца перавозкай велізарных колькасьцяў хімікатаў, найчасьцей нафтапрадуктаў, пальмавага алею, лою, каўстычнай соды, мэтанолу. Танкер „Хімічны суіскальнік“ на выяве прыстаў у порце Сэту (Эро, Францыя).

Энэргія актывацыі — энэргія, якую трэба пераадолець для зьдзяйсьненьня хімічнай рэакцыі. Іскры, атрыманыя ударам сталі аб крамень, даюць энэргію, дастатковую для ўзгараньня ў Бунзэнавым пальніку. Сіняе полымя будзе трымацца і пасьля зьнікненьня іскры, паколькі гарэньне цяпер падтрымлівае сябе само.
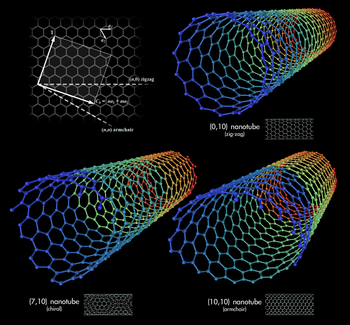
Вугляродныя нанатрубкі (ВНТ) — алятропныя адмены вугляроду. Яны могуць прымаць форму цыліндрычных малекулаў вугляроду і маюць незвычайныя асаблівасьці, дзякуючы якім могуць прымяняцца ў разнастайных галінах матэрыялазнаўства: нанатэхналёгіях, электроніцы, оптыцы. Яны валодаюць неймавернай трываласьцю, унікальнымі электрычнымі ўласьцівасьцямі і эфэктыўна праводзяць цяпло.

Тры палачкі чыстага ванаду ў розных ступенях атляненьня, створаныя ў працэсе Аркеля — дэ Бура, і кубік 1 см³ для параўнаньня.

Рэнтгенаўская крышталеграфія — аналітычны мэтад вызначэньня атамнай і малекулярнай структуры крышталяў. Час экспазыцыі для гэтага фатаздымку склаў 90 с, у які ўвайшлі 80 с, патрэбныя дыфрактомэтру на „сканаваньне“ крышталю.

Газаваньне адбываецца пры распушчэньні дыяксыду вугляроду ў вадзе або воднай рашчыне. Гэты працэс насычае газаваную і мінэральную ваду „шыпучкай“, у піве ўтварае пену, у шампанскім і пеністым віне — бурбалкі і выбух корку. На выяве паказанае ўсплыцьцё бурбалак дыяксыду вугляроду на паверхню газаванага прахаладжальнага напою.
Аэрагель — цьвёрды матэрыял малой шчыльнасьці, падобны да гелю, у якім вадкі складнік заменены газам. Выніковае рэчыва валодае некалькімі адметнымі ўласьцівасьцямі, найперш сваёй цеплаізаляцыйнай эфэктыўнасьцю. Аэрагелі маюць вельмі трывалую структуру, здольную вытрымліваць вагу ў 2000 большую за ўласную. Гэткая трываласьць дасягаецца дзякуючы дрэвападобнай мікраструктуры. На выяве цагліна масай 2,5 кг трымаецца на кавалку аэрагелю масай усяго 2,38 грамаў.
Алятропія — уласьцівасьць хімічнага рэчыва ўтвараць некалькі простых рэчываў розных фізычных формаў. Найбольшай колькасьцю такіх мадыфікацыяў валодае вуглярод. 8 зь іх прыведзеныя на выяве: алмаз (a), графіт (b), лонсдэйліт (c), бакмінстэрфулерэн (d), C540 (e), C70 (f), аморфны вуглярод (g) і аднасьценная нанатрубка (h).

Осм (Os) — хімічны элемэнт з атамным нумарам 76, плятынавы мэтал. Выкарыстоўваецца як кампанэнт звышцьвёрдых і зносаўстойлівых сплаваў (з ірыдам, рутэнам і інш.) для прыладабудаваньня, вырабу эталёнаў і г. д. На выяве — крышталі осму (2,2 г) чысьцінёю ≥ 99,99%, атрыманыя з дапамогай рэакцыі хімічнага пераносу ў атмасфэры хлёру.
Партал:Хімія/Абраная выява/25 Партал:Хімія/Абраная выява/25
Партал:Хімія/Абраная выява/26 Партал:Хімія/Абраная выява/26
Партал:Хімія/Абраная выява/27 Партал:Хімія/Абраная выява/27
Партал:Хімія/Абраная выява/28 Партал:Хімія/Абраная выява/28
Партал:Хімія/Абраная выява/29 Партал:Хімія/Абраная выява/29
Партал:Хімія/Абраная выява/30 Партал:Хімія/Абраная выява/30
Партал:Хімія/Абраная выява/31 Партал:Хімія/Абраная выява/31
Партал:Хімія/Абраная выява/32 Партал:Хімія/Абраная выява/32
Партал:Хімія/Абраная выява/33 Партал:Хімія/Абраная выява/33
Кандыдаты[рэдагаваць крыніцу]
Датычныя хімія/біяхімія/мінэралёгіі выявы можна прапанаваць тут.




